23 января 2025 года

Сравнительный анализ отдаленных онкологических результатов лечения рака предстательной железы высокоинтенсивной ультразвуковой абляцией и радикальной простатэктомией
Аннотация
Цель. Сравнить онкологическую эффективность при долгосрочном наблюдении высокоинтенсивной фокусированной ультразвуковой абляции (HIFU) и радикальной простатэктомии (РПЭ) при лечении пациентов с раком предстательной железы (РПЖ).
Методы. Проведен сравнительный ретроспективный анализ результатов лечения 194 пациентов, получившим HIFU-терапию и 150 пациентов, которым была выполнена РПЭ в период с 2008 по 2010 гг. в Самарском областном клиническом онкологическом диспансере. Для сравнения онкологической эффективности обоих методов лечения оценивались общая выживаемость, канцер-специфическая выживаемость и безрецидивная выживаемость. Биохимический рецидив диагностировался на основании критериев ASTRO/Phoenix. При статистическом анализе использовались одномерный логарифмический ранговый тест и метод Каплан-Мейера.
Результаты. Среднее время наблюдения в группах РПЭ и HIFU составило 14,5 и 15,2 года соответственно. 15-летняя общая, канцер-специфичная и безрецидивная выживаемости составили 28,3/77,7/53,7% в группе РПЭ и 48,0/79,4/69,8% в группе HIFU соответственно. Прогностически-значимыми факторами были: уровень ПСА до лечения, сумма Глисона. Результаты HIFU терапии в сравнении с РПЭ продемонстрировали более высокую общую выживаемость при сопоставимых значениях канцер-специфичной и безрецидивной выживаемостей.
Выводы. HIFU терапия может быть альтернативным методом лечения РПЖ для больных группы низкого и промежуточного риска прогрессии по D’Amico. Больные из группы высокого риска должны быть информированы о возможных повторных сеансах HIFU и/или адъювантном лечении. При долгосрочным наблюдении HIFU терапия показала сопоставимые показатели онкологической эффективности по сравнению с РПЭ при лечении больных с раком простаты.
Ключевые слова: рак простаты, HIFU, ультразвуковая абляция, радикальная простатэктомия.
Для цитирования:
Отдаленные онкологические результаты лечения рака предстательной железы высокоинтенсивной ультразвуковой абляцией и радикальной простатэктомией
В.А. Соловов1,2, А.А. Тюрин1,2
Медицинский университет РЕАВИЗ, г.Самара, Россия
Россия, 443030, г. Самара, ул. Чкалова, 100
ГБУЗ "Самарский областной клинический онкологический диспансер", г. Самара, Россия2
Россия, 443031, г. Самара, ул. Солнечная, 502
Введение
Рак предстательной железы является наиболее частым злокачественным заболеванием солидных органов и второй причиной смертности от рака среди мужчин во всем мире [1]. Общепринятые варианты лечения варьируют от активного наблюдения до простатэктомии и дистанционной лучевой терапии (ДЛТ), которые, несмотря на свои преимущества, все же связаны со значительным риском, и имеют высокий процент осложнений [2]. В связи с этим динамически развиваются малоинвазивные способы лечения РПЖ, такие как высокоинтенсивная фокусированная ультразвуковая абляция (HIFU), криоабляция. В рамках этой развивающейся парадигмы HIFU, благодаря своему ключевому преимуществу неинвазивности, стала действительной альтернативой «радикальным» способам лечения [3].
Использование высокоинтенсивного фокусированного ультразвука при лечении рака предстательной железы изучается с начала 1990-х годов. Кроме таких неоспоримых преимуществ метода, как неинвазивность и низкое количество послеоперационных осложнений, HIFU так же может являться опцией спасительного лечения при местном рецидиве РПЖ после РПЭ, ДЛТ или первичной HIFU-терапии [4]. Несмотря на всё возрастающее количество публикаций, свидетельствующих об удовлетворительных онкологических результатах HIFU терапии [5], продолжаются споры относительно эквивалентности метода по сравнению с «традиционными» вариантами лечения. Европейская ассоциация урологов, например, не рекомендует первичную HIFU вне клинических исследований из-за отсутствия достаточных долгосрочных проспективных и сравнительных данных с другими методами лечения [6]. И действительно, было опубликовано лишь несколько исследований, отражающих отдаленные онкологические результаты использования HIFU в лечении РПЖ, и, кроме того, недостаточно данных, сравнивающие HIFU с другими вариантами радикального лечения [7].
В связи с этим представляется весьма актуальным изучение клинического значения HIFU терапии при лечении РПЖ при длительном наблюдении. Целью настоящего исследования является сравнительный анализ отдаленных онкологических результатов лечения РПЖ HIFU-терапии и РПЭ.
Материалы и методы
Был проведен одноцентровой ретроспективный анализ результатов лечения пациентов, получивших HIFU-терапию и РПЭ в 2008-2010 гг, и сравнение их онкологических результатов. Исследование проводилось без какого-либо предварительного отбора пациентов, в него включены пациенты с неметастатическим РПЖ и сравнимыми онкологическими данными.
Критериями включения являлись: верифицированный рак предстательной железы cT1N0M0-cT3N0M0. Критериями исключения: метастатический РПЖ, обширные оперативные вмешательства на прямой кишке в анамнезе.
Пациенты, получавшие краткосрочную антиандрогенную терапию перед лечением, не были исключены из исследования. В таких случаях предлечебная ГТ не рассматривалась как неоадъювантная терапия, а назначалась индивидуально, чтобы обеспечить безопасность пациента, в том случае, когда решение о выборе метода лечения было отложено на несколько недель. Во всех случаях клинический диагноз основывался на предоперационных параметрах. Причины смерти, в том числе и от РПЖ, определены согласно раковому регистру. Период наблюдения определен как интервал между лечением и датой смерти/датой последней явки.
Пациенты группы HIFU и их последующее наблюдение
В исследование включены результаты лечения 194 больных, получившие HIFU-терапию. Большая часть пациентов этой группы либо отказались от хирургического лечения в пользу менее инвазивного способа, либо не подходили для РПЭ.
Все процедуры выполнялись с использованием аппарата Ablatherm®. Во всех случаях для обезболивания во время процедуры использовалась спинальная анестезия. Среднее время операции составило 146 мин (60-225). Средняя продолжительность госпитализации — 6 дней. Уретральный катетер удалялся в среднем на 5 сутки. Интраоперационных осложнений не было. У большинства пациентов перед лечением была выполнена трансуретральная резекция предстательной железы (ТУР) с целью уменьшения размеров предстательной железы и удаления кальцинатов. Наблюдение после HIFU включало в себя исследование уровня ПСА через 1, 3, 6, 12, 18 и 24 месяца, а затем — ежегодно. Онкологические результаты оценивались в соответствии с группами риска прогрессии по D’Amico [8]. Биохимический рецидив диагностировался в соответствии с критериями ASTRO/Phoenix [9]. Биопсии предстательной железы под контролем трансректального УЗИ проводились в случае положительного критерия Phoenix или в случае двухкратного повышения уровня ПСА менее, чем за полгода.
Пациенты группы РПЭ и их последующее наблюдение
В исследование были включены 150 пациентов, которым была выполнена открытая позадилонная РПЭ. Во всех случаях для обезболивания во время операции применялся эндотрахеальный наркоз. Среднее время операции составило 186 мин (80-245). Средняя продолжительность госпитализации — 14 дней. Уретральный катетер удалялся в среднем на 12 сутки. Критерием биохимического рецидива после простатэктомии считали уровень ПСА 0,2 нг/мл и более при двух последовательных измерениях [6].
Статистический анализ
Статистический анализ проводился с использованием SPSS версии 24.0. При сравнении параметрических переменных использовался t–критерий, в то время как для непараметрических переменных применялся U-критерий Манна-Уитни. Категориальные переменные сравнивались с использованием критерия хи-квадрат. Одномерный логарифмический ранговый тест использовался для сравнения РПЭ и HIFU, в то время как графики Каплана–Мейера использовались для графического представления. Для оценки влияния лечения на общую выживаемость, безрецидивную выживаемость, канцерспецифическую выживаемость была рассчитана многомерная регрессионная модель пропорциональных рисков Кокса для каждой конечной точки. Считалось, что значения р<0,05 указывают на статистическую значимость.
Результаты
Всего в исследование был включено 344 пациента, из которых 194 больной получил HIFU-терапию, 150 была выполнена РПЭ. Характеристики пациентов представлены в таблице 1.
Распределение пациентов с низким, промежуточным и высоким риском в соответствии с классификацией риска d’Amico показано в таблице 2 и статистически значимо не отличалось (p>0,05).
Таблица 1
Характеристика пациентов с РПЖ в зависимости от вида лечения
|
Значение показателя |
HIFU |
РПЭ |
Всего |
|---|---|---|---|
|
Кол-во пациентов |
194 |
150 |
344 |
|
Возраст медиана, лет |
69 (51-87) |
68 (52-82) |
69 (51-87) |
|
ПСА |
|
|
|
|
ПСА до лечения, нг/мл, n (%) <10 10 - <20 ≥20 |
103 (53,1) 68 (35,1) 23 (12,8) |
68 (57,1) 51 (42,9) 31 (20,7) |
171 (49,7) 119 (34,6) 54 (15,7) |
|
Сумма Глисон, n(%) ≤6 7 ≥8 |
143 (73,7) 32 (16,5) 19 (9,8) |
96 (80,7) 15 (12,6) 8 (6,7) |
239 (69,5) 33 (13,7) 27 (7,8) |
|
Стадия Т, n(%) T1 T2 T3 |
40 (20,6) 85 (43,8) 69 (35,6) |
40 (26,7) 69 (46,0) 41 (27,3) |
80 (23,6) 127 (36,9) 106 (30,8) |
|
Группа риска, n (%) Низкий Промежуточный Высокий |
48 (27,4) 71 (36,6) 75 (38,6) |
45 (30,0) 56 (37,3) 49 (32,7) |
93 (27,0) 127 (36,9) 124 (36,1) |
Максимальные сроки наблюдения составили 15 лет для всех групп пациентов. В таблице 2 представлены данные общей, безрецидивной и канцер-специфичной выживаемостей для группы пациентов, пролеченных HIFU-терапией, стратифицированных по методам лечения и классификациям риска по D’Amico. В таблице 3 показаны результаты лечения всех пациентов группы HIFU и РПЭ без деления на группы риска. Общая пятнадцатилетняя выживаемость для пациентов группы РПЭ составила 28,3%, канцерспецифическая (РПЖ) выживаемость – 77,7 %, а безрецидивная выживаемость составила 53,7 %; для группы HIFU – 48,0 %, 79,4 %, 69,8 %, соответственно. Кривые общей и безрецидивной выживаемостей для обеих групп, рассчитанные по методу Каплан-Мейера, представлены на рисунках 1 и 2 (значение ᵡ2 0,98 и 1,23 соответственно).
Таблица 2
Общая, безрецидивная, канцерспецифичная выживаемости в группе HIFU
|
Группа риска |
Общая выживаемость, % |
Канцерспецифичная выживаемость, % |
Безрецидивная выживаемость, % |
|
Низкий риск прогрессии |
56,1 |
93,75 |
85,42 |
|
Промежуточный риск прогрессии |
52,1 |
92,98 |
80,70 |
|
Высокий риск прогрессии |
37,9 |
84,85 |
69,70 |
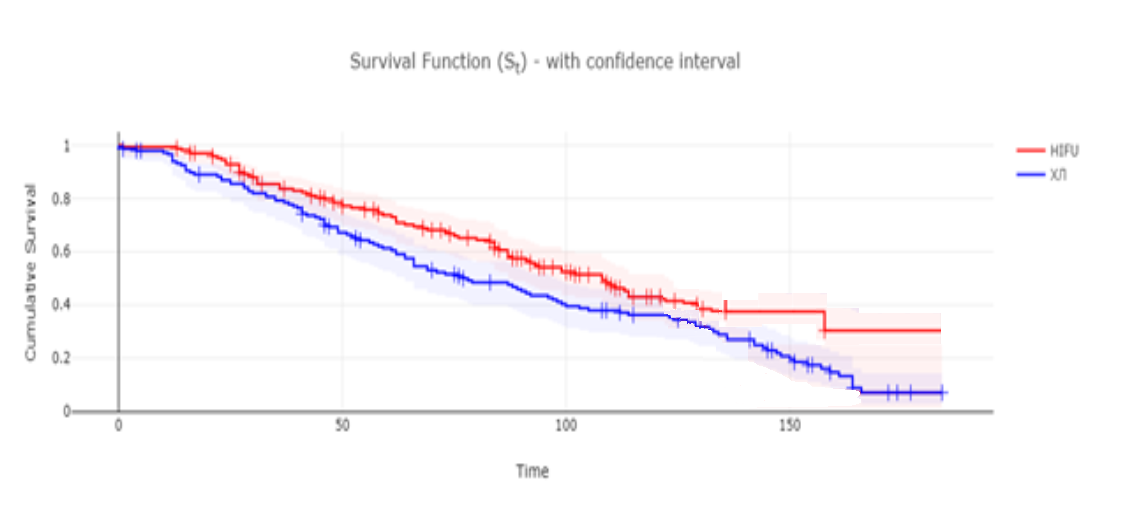
Рис. 1. Кривые общей выживаемости по Каплану-Мейеру для больных группы хирургического лечения и HIFU
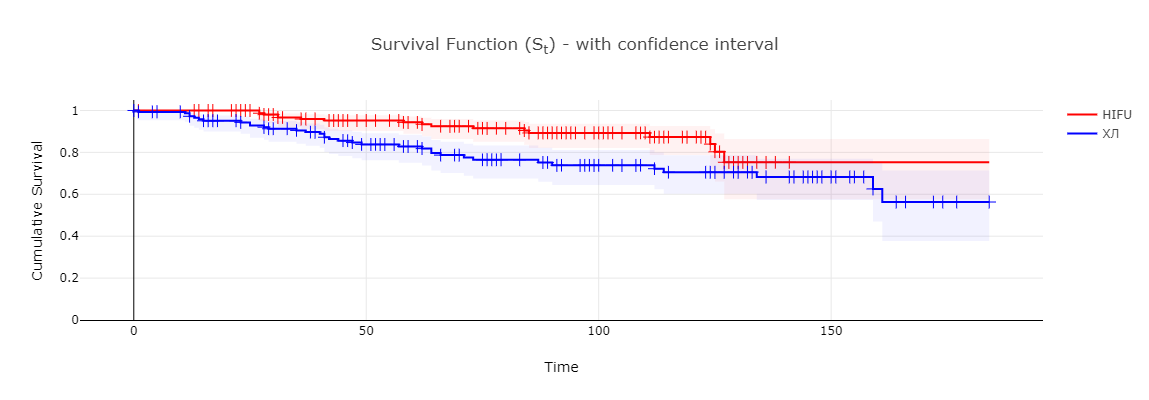
Рис. 2. Кривые безрецидивной выживаемости по Каплану-Мейеру для больных группы хирургического лечения и HIFU
В многофакторном регрессионном анализе Кокса (таблица 4) HIFU оказался независимым значимым прогностическим фактором снижения общей и канцероспецифической смертности по сравнению с РПЭ, при этом в случае с биохимическим рецидивом статистической значимости не отмечалось (p=0,072). Высокий балл Глисона и уровень ПСА были значимыми предикторами более высокой канцероспецифической смертности в группе HIFU. В группе пациентов с промежуточным и высоким риском прогрессии HIFU терапия значимо влияла на увеличение общей выживаемости по сравнению с РПЭ как показано в таблице 4. У пациентов с низким риском прогрессии статистически значимых отличий выявлено не было.
Таблица 4
Многофакторный регрессионный анализ Кокса: общая смертность, канцероспецифицеская смертность, биохимический рецидив
|
Прогностический фактор |
Общая смертность ОР (95% ДИ), p |
Канцерспецифичная смертность ОР (95% ДИ), p |
Биохимический рецидив ОР (95% ДИ), p |
|
РПЭ (по сравнению с HIFU) |
2,08 (1,32; 3,29), 0,001 |
3,99 (1,31, 12,07) 0,014 |
1,40 (0,96, 2,03) 0,071 |
|
ПСА |
0,99 (0,97, 1,01) 0,361 |
1,00 (0,97, 1,03) 0,832 |
1,01 (1,00, 1,01) 0,191 |
|
Глиссон |
1,05 (0,91, 1,22) 0,487 |
1,12 (0,82, 1,53) 0,487 |
1,13 (0,99, 1,29) 0,061 |
|
Риск прогрессии |
|
||
|
Низкий риск прогрессии |
1,55 (0,71, 1,54) 0,785 |
1,39 (0,64, 3,28) 0,411 |
0,96 (0,68, 1,35) 0,792 |
|
Промежуточный риск прогрессии |
1,06 (0,68, 1,61) 0,762 |
7,41 (1,63, 32,98) 0,008 |
1,03 (0,70, 1,58) 0,928 |
|
Высокий риск прогрессии |
1,71 (0,80, 3,52) 0,169 |
6,07 (0,91, 41,12) 0,071 |
1,69 (0,95, 2,89) 0,054 |
Обсуждение
Лечение пациентов с неметастатическим раком предстательной железы является предметом научных дискуссий. В последние десятилетия появились альтернативные методы лечения, направленные на достижение удовлетворительных онкологических результатов с минимальными побочными эффектами[10, 11, 12]. Среди таких методов HIFU-терапия стала популярной благодаря своей неинвазивности и минимальными осложнениями. В рамках этого развивавшегося тренда мы провели настоящее исследование для оценки отдаленных онкологических результатов HIFU терапии.
Насколько нам известно, в русскоязычной литературе данная публикация является первой, оценивающей долгосрочные онкологические результаты HIFU и РПЭ в лечении РПЖ.
Всего в анализ были включены результаты лечения 344 пациентов (194 получили HIFU терапию, 150 – РПЭ) со сроком наблюдения 15 лет. По результатам настоящего исследования было выявлено следующее. Во-первых, при длительном наблюдении канцероспецифическая выживаемость в группе HIFU сопоставима с группой РПЭ, 79,4 % и 77,7 %, соответственно. Во-вторых, безрецидивная выживаемость в группе HIFU выше, чем в группе РПЭ, 69,8 % и 53,7 %. В-третьих, наши данные продемонстрировали значительно более высокие показатели общей выживаемости в группе HIFU терапии (48,0 % против 28,3 %). Возможным объяснением этого является то, что HIFU терапия имеет ключевое преимущество – неинвазивность, в то время как РПЭ обладает большим количеством осложнений и побочных эффектов. Другой возможной причиной этих различий является то, что высокие показатели общей выживаемости после HIFU терапии могут быть обусловлены минимальными физической и психологической травмами во время лечения, с коротким периодом реабилитации. При этом высокие показатели безрецидивной выживаемости после ультразвуковой абляции могут быть связаны со стимуляцией противоопухолевого иммунного ответа [13].
В ряде работ было показано [5], что HIFU представляется разумной альтернативой для пациентов с локализованным РПЖ низкого риска прогрессии, однако наше исследование демонстрирует весьма воодушевляющие результаты и для больных групп промежуточного и даже высокого риска: показатели РПЖ-специфичной и безрецидивной выживаемости в сравнении с аналогичными контрольными точками в группе РПЭ оказались сопоставимыми.
В 2024 году были представлены данные первого проспективного исследования, в котором был проведен сравнительный анализ онкологической эффективности HIFU терапии и радикальной простатэктомии. В исследование были включены результаты лечения 3328 пациентов с локализованным РПЖ, средний срок наблюдения составил 30 месяцев. Исследователи пришли к выводу, что HIFU и РПЭ имеют сопоставимую онкологическую эффективность, при этом HIFU продемонстрировало отличные функциональные результаты [14].
В опубликованном недавно систематическом обзоре и мета-анализе группой экспертов было показано, что HIFU терапия имеет сопоставимые показатели биохимической безрецидивной, раково-специфической, общей выживаемости (58 %, 96 %, 63 %) по сравнению с традиционными методами при лечении локализованного РПЖ через 10 лет наблюдения. При этом HIFU обеспечивает превосходные функциональные результаты и имеет минимальное количество осложнений [15].
Наши же долгосрочные данные не опровергают предыдущие среднесрочные результаты и дают дополнительную информацию за пределами 10-летнего периода наблюдения. Сильные стороны нашего исследования, безусловно, заключаются в большом количестве пациентов и длительном периоде наблюдения. При этом мы включали пациентов всех категорий риска без предварительного отбора. Представленные данные подтверждают, что HIFU является безопасным вариантом лечения, в том числе и для пациентов высокого риска прогрессии. В этом контексте наши результаты дополняют существующие публикации, рекомендующие HIFU для лечения РПЖ у пациентов низкого и промежуточного риска прогрессии [16, 17, 18].
Однако, мы не предоставляем данные о функциональных результатах и осложнениях, поскольку это выходит за рамки данного исследования. Однако понимание качества жизни в долгосрочной перспективе является важнейшим вопросом при планировании лечения. Несмотря на онкологические преимущества HIFU-терапии, неинвазивность метода может быть еще одним принципиальным моментом в процессе принятия решений.
Между тем, настоящее исследования имеет ряд ограничений. Во-первых, настоящее исследование было одноцентровым, ретроспективным. Во-вторых, биохимический рецидив после HIFU терапии определялся согласно критериям ASTRO/Phoenix, которые основаны на анализе значения ПСА после ДЛТ. При этом учитывалось то, что большинство предыдущих исследователей также оценивали эффективность HIFU с помощью этих критериев. В-третьих, хорошие онкологические результаты могут быть следствием того, что все пациенты получали лечение в одном крупном онкологическом центре с большим опытом проведения HIFU-терапии. И, наконец, включение в исследование больных, получавших неоадъювантную АДТ, так же могло исказить результаты, но мы считаем, что учитывая краткосрочность неоадъювантной АДТ, этим фактором можно пренебречь.
Заключение
HIFU терапия может быть альтернативным методом лечения РПЖ для больных группы низкого и промежуточного риска прогрессии. Больные из группы высокого риска должны быть информированы о возможных повторных сеансах HIFU и/или адъювантном лечении. При долгосрочном наблюдении HIFU терапия показала сопоставимые показатели онкологической эффективности по сравнению с РПЭ при лечении больных с раком простаты. Метод позволяет добиться весьма обнадеживающих онкологических результатов при всех плюсах, связанных с его неинвазивностью. Разумеется, необходимо больше многоцентровых проспективных рандомизированных исследований с большим числом больных, чтобы подтвердить наши данные и оценить долгосрочную эффективность HIFU-терапии.
Список литературы
- Siegel RL, Miller KD, Fuchs HE, Jemal A. Cancer statistics, 2022. CA Cancer J Clin. 2022;72(1):7-33. doi:10.3322/caac.21708
- Carlsson S, Benfante N, Alvim R, et al. Long-Term Outcomes of Active Surveillance for Prostate Cancer: The Memorial Sloan Kettering Cancer Center Experience. J Urol. 2020;203(6):1122-1127. doi:10.1097/JU.0000000000000713
- Wang A, O'Connor LP, Yerram NK, et al. Focal therapy for prostate cancer: recent advances and future directions. Clin Adv Hematol Oncol. 2020;18(2):116-125.
- Chaussy CG, Thüroff S. High-Intensity Focused Ultrasound for the Treatment of Prostate Cancer: A Review. J Endourol. 2017 Apr;31(S1):S30-S37. doi: 10.1089/end.2016.0548. Epub 2017 Mar 29. PMID: 28355119.
- Dickinson L, Arya M, Afzal N, Cathcart P, Charman SC, Cornaby A, Hindley RG, Lewi H, McCartan N, Moore CM, Nathan S, Ogden C, Persad R, van der Meulen J, Weir S, Emberton M, Ahmed HU. Medium-term Outcomes after Whole-gland High-intensity Focused Ultrasound for the Treatment of Nonmetastatic Prostate Cancer from a Multicentre Registry Cohort. Eur Urol. 2016 Oct;70(4):668-674. doi: 10.1016/j.eururo.2016.02.054. Epub 2016 Mar 4. PMID: 26951947.
- Mottet N, Bellmunt J, Bolla M, Briers E, Cumberbatch MG, De Santis M, Fossati N, Gross T, Henry AM, Joniau S, Lam TB, Mason MD, Matveev VB, Moldovan PC, van den Bergh RCN, Van den Broeck T, van der Poel HG, van der Kwast TH, Rouvière O, Schoots IG, Wiegel T, Cornford P. EAU-ESTRO-SIOG Guidelines on Prostate Cancer. Part 1: Screening, Diagnosis, and Local Treatment with Curative Intent. Eur Urol. 2017 Apr;71(4):618-629. doi: 10.1016/j.eururo.2016.08.003. Epub 2016 Aug 25. PMID: 27568654.
- Thüroff S, Chaussy C. Evolution and outcomes of 3 MHz high intensity focused ultrasound therapy for localized prostate cancer during 15 years. J Urol. 2013 Aug;190(2):702-10. doi: 10.1016/j.juro.2013.02.010. Epub 2013 Feb 13. PMID: 23415962.
- D'Amico AV, Whittington R, Malkowicz SB, Schultz D, Blank K, Broderick GA, Tomaszewski JE, Renshaw AA, Kaplan I, Beard CJ, Wein A. Biochemical outcome after radical prostatectomy, external beam radiation therapy, or interstitial radiation therapy for clinically localized prostate cancer. JAMA. 1998 Sep 16;280(11):969-74. doi: 10.1001/jama.280.11.969. PMID: 9749478.
- Roach M 3rd, Hanks G, Thames H Jr, Schellhammer P, Shipley WU, Sokol GH, Sandler H. Defining biochemical failure following radiotherapy with or without hormonal therapy in men with clinically localized prostate cancer: recommendations of the RTOG-ASTRO Phoenix Consensus Conference. Int J Radiat Oncol Biol Phys. 2006 Jul 15;65(4):965-74. doi: 10.1016/j.ijrobp.2006.04.029. PMID: 16798415.
- Guang ZLP, Kristensen G, Røder A, Brasso K. Oncological and Functional Outcomes of Whole-Gland HIFU as the Primary Treatment for Localized Prostate Cancer: A Systematic Review. Clin Genitourin Cancer. Published online April 25, 2024. doi:10.1016/j.clgc.2024.102101
- Bründl J, Osberghaus V, Zeman F, et al. Oncological Long-term Outcome After Whole-gland High-intensity Focused Ultrasound for Prostate Cancer-21-yr Follow-up. Eur Urol Focus. 2022;8(1):134-140. doi:10.1016/j.euf.2020.12.016
- Rosenhammer B, Ganzer R, Zeman F, Näger T, Fritsche HM, Blana A, Burger M, Bründl J. Oncological long-term outcome of whole gland HIFU and open radical prostatectomy: a comparative analysis. World J Urol. 2019 Oct;37(10):2073-2080. doi: 10.1007/s00345-018-2613-z. Epub 2019 Jan 2. PMID: 30603784
- Karwacki J, Kiełbik A, Szlasa W, Sauer N, Kowalczyk K, Krajewski W, Saczko J, Kulbacka J, Szydełko T, Małkiewicz B. Boosting the Immune Response-Combining Local and Immune Therapy for Prostate Cancer Treatment. Cells. 2022 Sep 7;11(18):2793. doi: 10.3390/cells11182793. PMID: 36139368; PMCID: PMC9496996.
- Parry MG, Sujenthiran A, Nossiter J, Morris M, Berry B, Nathan A, Aggarwal A, Payne H, van der Meulen J, Clarke NW. Prostate cancer outcomes following whole-gland and focal high-intensity focused ultrasound. BJU Int. 2023 Nov;132(5):568-574. doi: 10.1111/bju.16122. Epub 2023 Jul 25. PMID: 37422679.
- Rischmann PJ, Coloby P, Chevallier T, Houede N, Villers A, Ploussard G. P2-06 HIFI TRIAL: HIFU VS RADICAL PROSTATECTOMY FOR LOCALIZED PROSTATE CANCER IN 3328 CASES. FINAL RESULTS. Journal of Urology [Internet]. 2024 May 1 [cited 2024 Jun 4];211(5S2):e4. doi.org/10.1097/01.JU.0001015816.87470.c9.06
- Hamdy FC, Donovan JL, Lane JA, Metcalfe C, Davis M, Turner EL, Martin RM, Young GJ, Walsh EI, Bryant RJ, Bollina P, Doble A, Doherty A, Gillatt D, Gnanapragasam V, Hughes O, Kockelbergh R, Kynaston H, Paul A, Paez E, Powell P, Rosario DJ, Rowe E, Mason M, Catto JWF, Peters TJ, Oxley J, Williams NJ, Staffurth J, Neal DE; ProtecT Study Group. Fifteen-Year Outcomes after Monitoring, Surgery, or Radiotherapy for Prostate Cancer. N Engl J Med. 2023 Apr 27;388(17):1547-1558. doi: 10.1056/NEJMoa2214122. Epub 2023 Mar 11. PMID: 36912538.
- van der Poel HG, van den Bergh RCN, Briers E, Cornford P, Govorov A, Henry AM, Lam TB, Mason MD, Rouvière O, De Santis M, Wiegel T, Willemse PM, van Poppel H, Mottet N. Reply to Massimo Valerio, Mark Emberton, and Hashim U. Ahmed's Letter to the Editor re: Henk G. van der Poel, Roderick C.N. van den Bergh, Erik Briers, et al. Focal Therapy in Primary Localised Prostate Cancer: The European Association of Urology Position in 2018. Eur Urol 2018;74:84-91. Eur Urol. 2019 Feb;75(2):e23-e24. doi: 10.1016/j.eururo.2018.08.043. Epub 2018 Sep 17. PMID: 30237024.
- Deivasigamani S, Kotamarti S, Rastinehad AR, et al. Primary Whole-gland Ablation for the Treatment of Clinically Localized Prostate Cancer: A Focal Therapy Society Best Practice Statement. Eur Urol. 2023;84(6):547-560. doi:10.1016/j.eururo.2023.06.013
Подпишитесь на нашу рассылку о новинках и акциях

Спасибо за подписку!
Наши менеджеры свяжутся с вами в течение дня
